Definition des normalen und pathologischen pädiatrischen und neonatalen EKGs
Das neonatale und pädiatrische EKG wird nach den gleichen Prinzipien interpretiert wie das EKG bei Erwachsenen. Das EKG muss immer mit einem systematischen Ansatz interpretiert werden, um die Wahrscheinlichkeit zu minimieren, dass signifikante Abnormalitäten übersehen werden. Die folgenden Parameter müssen in chronologischer Reihenfolge beurteilt werden:
- Herzfrequenz
- Rhythmus
- P-Welle
- PQ-Intervall
- QRS-Komplex
- ST-Strecke
- T-Welle
- U-Welle
- QT (QTc) -Intervall
Pädiatrische und neonatale EKGs unterscheiden sich deutlich – in Bezug auf Rhythmus, Morphologie, Normalbefunde, Normalvarianten usw. – von EKGs bei Erwachsenen. Es ist entscheidend, sich mit Normalbefunden, Normalvarianten und Pathologien bei Neugeborenen, Säuglingen und während der Kindheit vertraut zu machen. Im Folgenden wird jeder der neun oben aufgeführten Parameter erläutert. Viele der unten genannten Diagnosen werden in anderen Kapiteln ausführlich diskutiert, welche im gesamten Text entsprechend verlinkt sind.
Herzfrequenz
In der ersten Lebenswoche beträgt die Herzfrequenz ungefähr 120 Schläge pro Minute. Die Herzfrequenz steigt dann in den ersten 1 bis 2 Monaten auf etwa 150 Schläge pro Minute und sinkt dann allmählich auf etwa 120 Schläge pro Minute im Alter von 6 Monaten. Nach 12 Monaten sinkt die Herzfrequenz stetig und im Alter von 10 Jahren ist die Herzfrequenz dieselbe wie beim Erwachsenen. Diese Altersschwankungen der Herzfrequenz sind auf Schwankungen der Aktivität des autonomen Nervensystems und auf Veränderungen der Automatizität im Sinusknoten zurückzuführen.
Rhythmus
Normaler Rhythmus
Ein Rhythmus ist definiert als drei aufeinanderfolgende Schläge mit identischen Wellenformen im EKG. Die Gleichheit der Wellenformen zeigt an, dass der Impuls den gleichen Ursprung hat. Der sinoatriale (SA-) Knoten ist unter normalen Umständen der Herzschrittmacher und der Rhythmus wird als Sinusrhythmus bezeichnet. Daher ist der Sinusrhythmus der normale Herzrhythmus. Der Sinusrhythmus auch bei allen pädiatrischen Patienten ist der normale Rhythmus. Der Sinusrhythmus ist durch folgende Kriterien definiert:
- Regelmäßiger Rhythmus mit einer ventrikulären Frequenz innerhalb des altersspezifischen Normalintervalls.
- P-Welle mit konstanter Morphologie, die jedem QRS-Komplex vorausgeht.
- Die P-Welle ist in Ableitung II (und auch I und aVF) positiv.
Arrhythmien
Sinustachykardie
Eine Sinustachykardie besteht, wenn die Herzfrequenz über der oberen Normalgrenze liegt und kann bei Kindern 240 Schläge pro Minute übersteigen. Wie im Sinusrhythmus geht eine P-Welle jedem QRS-Komplex voraus und die P-Welle ist in Ableitung II positiv.
Eine Sinustachykardie gilt immer als pathologisch und die zugrunde liegende Ursache muss untersucht werden. Schmerzen, Infektionen, Medikamente, Fieber, Hypovolämie, Dehydration, Anämie, Hyperthyreose und Myokarditis sind häufige Ursachen. Die Behandlung der zugrunde liegenden Ursache sollte die Sinustachykardie beheben.
Sinusarrhythmie
Eine Sinusarrhythmie (respiratorische Sinusarrhythmie) erfüllt alle Kriterien für den Sinusrhythmus, mit der Ausnahme, dass der Rhythmus leicht unregelmäßig ist. Das Phänomen erklärt sich durch Herzfrequenzschwankungen, die durch die Atmung verursacht werden. Die Herzfrequenz steigt während der Inspiration (aufgrund des verminderten Vagustonus) und nimmt während des Expiration ab (aufgrund eines erhöhten Vagustonus). Dies führt zu einem leicht unregelmäßigen Rhythmus.
Die Sinusarrhythmie tritt bei der Mehrheit der gesunden pädiatrischen Patienten auf. P-Wellen gehen allen QRS-Komplexen voraus und das PQ-Intervall ist konstant. Obwohl die Sinusarrhythmie bei pädiatrischen Patienten ausgeprägt sein kann, gilt sie als benigner Befund.
In der Regel ist die Sinusarrhythmie bei älteren Kindern ausgeprägter, da sie eine niedrigere Herzfrequenz haben. Ältere Kinder können gebeten werden, den Atem anzuhalten, was zur Aufhebung der Sinusarrhythmie führen sollte.
Sinuspause
Eine Sinuspause tritt auch bei Kindern auf. Sie äußert sich in Form von plötzlichen Verlängerungen im P-P-Intervall (ohne Bezug zur Atmung). Etwa die Hälfte aller Neugeborenen weisen Sinuspausen auf (Southall et al.) und dies gilt als Normalbefund. Eine Sinuspause tritt bei etwa 10% der Jungendlichen auf. Sie gilt als Normalbefund, wenn sie einige Male am Tag auftritt. Die Pause darf 2 Sekunden nicht überschreiten. Wenn die Pause 2 Sekunden überschreitet (> 2,5 Sekunden sind als Sinusarrest definiert) oder wenn Pausen häufig oder konsekutiv auftreten, kann dies durch eine Sinusknotendysfunktion, einen hypersensitiven Karotisreflex oder einen überaktiven Vagusnerv erklärt werden (Abbildung 4).
Kinder mit hypersensitiven Karotisreflex oder überaktivem Vagusnerv können viele Sinusarreste/Sinuspausen haben. Die Personen mit überaktivem Vagusnerv können während des Schlafes, während des Stuhlgangs, bei Nahrungsaufnahme und in anderen Situationen mit übermäßiger Vagusbelastung eine Sinuspause/Sinusarrest erfahren.
Ektopischer Vorhofrhythmus
Ein ektopischer Vorhofrhythmus ist bei Kindern häufig. Dieser Rhythmus ist durch abnormale P-Wellen in Ableitung II gekennzeichnet, insbesondere retrograde (negative) P-Wellen. Gesunde Kinder, die mit einem Holter-EKG überwacht werden, zeigen häufig Perioden mit ektopischen Vorhofrhythmus. Etwa 20% aller Kinder weisen einen ektopischen supraventrikulären Rhythmus auf (Goodacre, BMJ, 2002); diese Episoden dauern selten länger als 1 Minute und treten gehäuft im Schlaf auf.
Ein ektopischer Vorhofrhythmus mit variierender P-Wellen-Morphologie deutet darauf hin, dass es mehrere ektopische Herde gibt. Solche Arrhythmien werden als wandernder atrialer Herzschrittmacher (engl. wandering atrial pacemaker) bezeichnet, wenn die ventrikuläre Rate unter 100 Schläge pro Minute liegt, und als multifokale Vorhoftachykardie (engl. multifocal atrial tachycardia, MAT), wenn die ventrikuläre Rate ≥100 Schläge pro Minute beträgt.
Andere Tachyarrhythmien
Tachyarrhythmien bei pädiatrischen Patienten werden auf die gleiche Weise wie bei Erwachsenen diagnostiziert (siehe Diagnose und Management von Tachyarrhythmien/Tachykardie). Die AV-Knoten-Reentrytachykardie und AV-Reentrytachykardie sind nach der Sinustachykardie die häufigsten Ursachen für eine Schmalkomplextachykardie (QRS-Intervall <0,12 Sek). Vorhofflimmern und Vorhofflattern sind selten und weisen auf eine strukturelle Herzerkrankung hin (Vorhofflimmern und -flattern sind auch nach Herzoperationen häufig).
Junktionale Tachykardie (Junktionale ektopische Tachykardie, JET) kommt ebenfalls bei Kindern vor.
Insgesamt sind etwa 90% aller Tachyarrhythmien bei pädiatrischen Patienten supraventrikulär. Die restlichen 10% sind ventrikulär und wie bei Erwachsenen ernster. Etwa die Hälfte der Patienten mit rezidivierenden Tachyarrhythmien haben nachweislich ein strukturell normales Herz. Beim Rest sind strukturelle Herzkrankheiten und das Wolff-Parkinson-White-Syndrom (Präexzitation) die häufigsten Ursachen.
Tachyarrhythmien mit einem breiten QRS-Komplex (QRS-Intervall ≥ 0,12 Sek) sollten als ventrikuläre Tachykardie angesehen werden, bis Gegenteiliges nachgewiesen wird. Wie bei Erwachsenen können Tachyarrhythmien mit breiten QRS-Komplexen jedoch auch supraventrikulär sein, wobei der breite QRS-Komplex z.B. durch einen Schenkelblock, durch Hyperkaliämie oder eine aberrante Überleitung verursacht werden kann. Die Methoden zur Unterscheidung zwischen ventrikulärer und supraventrikulärer Tachykardie mit breitem QRS-Komplex sind die gleichen wie bei Erwachsenen.
Die ventrikuläre Tachykardie bei Kindern kann entweder monomorph (z.B. bei Kardiomyopathie, angeborener Herzkrankheit usw.) oder polymorph (z.B. beim Long-QT-Syndrom [LQTS], bei familiärer katecholaminerger polymorpher ventrikulärer Tachykardie und beim Brugada-Syndrom) sein.
Es sollte beachtet werden, dass Tachyarrhythmien bei Kindern sehr hohe ventrikuläre Frequenzen aufweisen können. Bei Neugeborenen und Säuglingen ist eine ventrikuläre Frequenz von bis zu 330 Schläge pro Minute möglich und > 200 Schläge pro Minute sind häufig. Kleinkinder und Jugendliche haben normalerweise Frequenzen von 150-250 Schläge pro Minute. Pädiatrische Patienten, ähnlich wie Erwachsene, können Tachyarrhythmien über lange Zeit ertragen, aber eine Dekompensation kann ohne Vorwarnung auftreten, insbesondere bei Patienten mit struktureller Herzerkrankung.
Verabreichung von Adenosin bei pädiatrischen Patienten
Dosierung: intravenöses oder intraossäres Adenosin 0,1 mg/kg, verabreicht als schneller Bolus (maximal 6 mg). Wenn dies nicht erfolgreich ist, kann eine zweite Dosis von 0,2 mg/kg als schneller Bolus (maximal 12 mg) verabreicht werden. Auf jeden Bolus folgt sofort ein Bolus mit Kochsalzlösung. Nebenwirkungen sind Flushing, Brustbeschwerden, eine vorübergehende Asystole oder Bradykardie. Bei Patienten, die Dipyridamol oder Carbamazepin einnehmen, sollte die halbe Dosis verwendet werden, die beide die Wirkung von Adenosin verstärken. Die halbe Dosis wird auch bei Herztransplantationspatienten und bei Verwendung eines zentralen Zugangs verwendet.
Adenosin ist die primäre Wahl zur Behandlung einer stabilen Schmalkomplextachykardie. Bei Verwendung als schneller Bolus verlangsamt Adenosin die Überleitung im Herzen, insbesondere im AV-Knoten. Dies kann die Reentry-Kreisläufe terminieren und den Sinusrhythmus wiederherstellen.
Betablocker und Verapamil sollten nicht zur Behandlung von Tachyarrhythmien angewendet werden. Betablocker haben keine antiarrhythmische Wirkung und Verapamil kann Tachyarrhythmien bei akzessorischen Leitungsbahnen (d.h. WPW-Syndrom) verschlimmern.
Vagale Manöver können die gleiche Wirkung wie Adenosin haben und können vor der Verabreichung von Adenosin versucht werden. Es gibt mehrere vagale Manöver (Karotismassage, Valsalva-Manöver, kaltes Wasser ins Gesicht usw.).
Adenosin sollte nur von erfahrenem Personal verabreicht werden, das in Reanimationsbereitschaft ist. Adenosin wird unter kontinuierlicher EKG-Überwachung verabreicht.
Synchronisierte Kardioversion
Eine akute Kardioversion wird bei bevorstehendem oder manifestem Kreislaufkollaps durchgeführt. Vorhandenes Bewusstsein ist eine Kontraindikation für eine Kardioversion. Eine Anästhesie kann notwendig sein, um eine Kardioversion durchzuführen.
Sinusbradykardie
Eine Sinusbradykardie bedeutet, dass die Kriterien für den Sinusrhythmus erfüllt sind, die Herzfrequenz jedoch unter der unteren (altersbedingten) Normalgrenze liegt. Eine Bradykardie ist im Allgemeinen alarmierender als eine Tachykardie. Die Ursachen für eine Sinusbradykardie sind wie folgt: Hypoxie, Hypothermie, Hypothyreose, AV-Block, erhöhter intrakranieller Druck, LQTS, Meningitis, Azidose und Sepsis. Stabile Patienten mit Sinusbradykardie sollten zunächst mit einem Holter-EKG untersucht werden.
Supraventrikuläre und ventrikuläre Extrasystolen
Supraventrikuläre Extrasystolen treten bereits von der Geburt auf. Supraventrikuläre Extrasystolen sind im ersten Lebensjahr häufiger als ventrikuläre Extrasystolen. Die meisten gesunden Kinder haben nur eine oder einige wenige Extrasystolen pro Stunde, welche normalerweise bei körperlicher Aktivität verschwinden (was darauf hinweist, dass sie benigne sind).
Ventrikuläre Extrasystolen werden bei 30% der gesunden Kinder beobachtet. In der Regel sind diese Extrasystolen unifokal (d.h. alle Extrasystolen haben ein identisches QRS-Aussehen). Konsekutive ventrikuläre Extrasystolen und multifokale ventrikuläre Extrasystolen (d.h. die Extrasystolen haben ein unterschiedliches QRS-Aussehen) sind seltener. Extrasystolen in Bigemini, Trigemini und Quadrigemini treten ebenfalls auf. Bei der überwiegenden Mehrheit der gesunden Menschen beträgt die Anzahl der ventrikulären Extrasystolen <50 Schläge pro Tag. Diese Extrasystolen sollten während körperlicher Betätigung verschwinden.
P-Welle
Das Aussehen, die Amplitude und die Dauer der P-Welle ändern sich im Laufe des Lebens sehr wenig. Referenzwerte für Erwachsene und Kinder sind praktisch identisch. Die Amplitude der P-Welle sollte <2,5 mm (98. Perzentile) in Ableitung II und <1,5 mm in Ableitung V1 betragen.
Abnorme P-Wellen: Vorhofabnormalitäten
P pulmonale
Wenn die Amplitude der P-Welle 2,5 mm in Ableitung II oder 1,5 mm in Ableitung V1 überschreitet, sollte eine Vergrößerung des rechten Vorhofs vermutet werden. Dieser Befund wird als P pulmonale bezeichnet.
P mitrale
Eine linksatriale Vergrößerung sollte vermutet werden, wenn die Dauer der P-Welle verlängert ist, insbesondere wenn die P-Welle in Ableitung II zwei Höcker hat und in Ableitung V1 eindeutig biphasig ist.
P mitrale und P pulmonale sind in Abbildung 1 dargestellt.

PQ-Intervall
Der durchschnittliche PQ-Intervall bei Geburt beträgt 107 ms (Davignon et al.). Aufgrund von Veränderungen des sympathischen und parasympathischen Tonus sinkt das PQ-Intervall im Alter von 1 Monat auf 98 ms (Mittelwert). Das nachfolgende Vorhofwachstum und Veränderungen im autonomen Gleichgewicht führen zu einem sukzessiven Anstieg des PQ-Intervalls nach einem Monat.
Präexzitation und atrioventrikulärer (AV-) Block
Die Beurteilung des PQ-Intervalls ist bei pädiatrischen und erwachsenen Patienten gleich. Ein verkürztes PR-Intervall (d.h. PR-Intervall kürzer als das zweite Perzentil, siehe Normalwerte für das pädiatrische EKG) deutet auf eine Präexzitation hin. Die Prinzipien der Präexzitation bei Kindern sind die gleichen wie bei Erwachsenen. Einzelheiten finden sich im Kapitel Präexzitation und Wolff-Parkinson-White-Syndrom.
Ein verlängerter PQ-Intervall deutet auf einen AV-Block hin. Lange PR-Intervalle im Schlaf sind jedoch normal; das PQ-Intervall kann im Schlaf 200 ms überschreiten, was durch den hohen Vagustonus bei Kindern erklärt wird. Daher ist ein AV-Block ersten Grades bei pädiatrischen Patienten im Schlaf normal. Einzelne Episoden eines AV-Block ersten Grades tagsüber gelten bei Kindern ebenso als normal. Häufige und rezidivierende Episoden eines AV-Block ersten Grades sind jedoch pathologisch. Es gibt mehrere Ursachen für einen AV-Block ersten Grades bei Kindern, z.B. Perikarditis, Myokarditis, Perimyokarditis, Ebstein-Anomalie, Endokardkissendefekt, atrialer Septumdefekt (ASD), Digoxin und Hyperkaliämie.
Ein AV-Block zweiten Grades Typ 1 (Wenckebach-Block) gilt als Normalbefund im Schlaf und bei einzelnen Episoden am Tage. Häufigere Episoden deuten auf eine Grunderkrankung hin.
Ein AV-Block dritten Grades (kompletter Herzblock) ist selten und meist ein Zeichen für eine signifikante Herzerkrankung. Angeborene (strukturelle) Herzkrankheiten sind eine der häufigsten Ursachen für einen AV-Block dritten Grades bei Kindern. Der postnatale Beginn eines AV-Block dritten Grades sollte ebenfalls zum Verdacht auf einen autoimmunen AV-Block führen. Mutterliche Ro-SSA- und La-SSB-Autoantikörper (häufig bei Bindegewebserkrankungen) können über die Plazenta auf den Fötus übertragen werden. Diese Autoantikörper zielen auf das Reizleitungssystem ab, was zu einem AV-Block dritten Grades führen kann. Andere häufige Ursachen für einen AV-Block dritten Grades sind Myokarditis und Herzoperationen, die den unteren Bereich der Vorhöfe, das atriale Septum oder das obere Ventrikelseptum betreffen. Die Mortalität bei angeborenem AV-Block dritten Grades ist bei Neugeborenen und Säuglingen hoch.
Dem vollständigen AV-Block kann ein AV-Block ersten und zweiten Grades vorausgehen, weshalb empfohlen wird, bei Patienten mit AV-Block ersten oder zweiten Grades wiederholt EKGs zu schreiben. Bei einem Kind mit angeborenem AV-Block sollte bei der Mutter ebenfalls ein EKG geschrieben werden. Eine Analyse von Ro-SSA- und La-SSB-Antikörpern ist ebenfalls indiziert. Bei Neugeborenen mit AV-Block zweiten oder dritten Grades sollten gründliche Untersuchungen, einschließlich bildgebender Verfahren, durchgeführt werden.
Die EKG-Kriterien für einen AV-Block bei Kindern sind identisch mit den Kriterien bei Erwachsenen, wobei die einzige Ausnahme die obere Normalgrenze für das PQ-Intervall ist.
Ursachen für ein kurzes PQ-Intervall bei pädiatrischen Patienten
- Präexzitation (Wolff-Parkinson-White-Syndrom)
- Morbus Pompe
- Morbus Fabry
- Ektopischer Vorhofrhythmus mit einem Fokus in der Nähe des AV-Knoten
Ektopische Vorhofrhythmen, die in der Nähe des AV-Knotens entstehen, können zu einem kurzen PQ-Intervall führen, einfach weil der Abstand zwischen dem AV-Knoten und dem ektopen Fokus kurz ist.
Es ist zu beachten, dass in einigen Fällen ektopische Vorhofschläge oder Vorhofrhythmen im Vergleich zu Sinusschlägen ein längeres PQ-Intervall aufweisen können, was dadurch erklärt wird, dass das AV-System bei schnellen atrialen Depolarisationen erschöpft werden kann.
Akzessorische Leitungsbahnen und Präexzitation
Der atrioventrikuläre (AV-) Knoten und das His-Bündel sind normalerweise die einzige Kommunikation zwischen den Vorhöfen und den Ventrikeln. Der atriale Impuls muss den AV-Knoten passieren, der den Impuls aufgrund seiner langsamen Überleitung verzögert, bevor der Impuls die Ventrikel erreicht. Einige Personen besitzen jedoch eine zusätzliche Leitungsbahn zwischen den Vorhöfen und den Ventrikeln. Solche Leitungsbahnen können den atrialen Impuls direkt auf die Ventrikel überleiten, ohne das AV-System zu passieren. Diese Leitungsbahnen werden als akzessorische Leitungsbahnen (oder Kentbündel) bezeichnet. Akzessorische Leitungsbahnen sind embryologische Überreste und können den Impuls von den Vorhöfen zu den Ventrikeln (antegrade Richtung), von den Ventrikeln zum Vorhof (retrograd Richtung), oder in beide Richtungen leiten.
Akzessorische Leitungsbahnen haben eine rapide Reizweiterleitung, was bedeutet, dass jeder Impuls, der die akzessorischen Leitungsbahnen erreicht, unverzüglich direkt in die Ventrikel gelangen kann. Daher können die Ventrikel früher als erwartet erregt (depolarisiert) werden, was als Präexzitation bezeichnet wird. Dies zeigt sich an drei Merkmalen im EKG und die Kombination dieser Merkmale ist einzigartig für die Präexzitation:
- Verkürztes PQ-Intervall: Das PQ-Intervall ist kürzer als die altersspezifische untere Normalgrenze.
- Deltawelle: Die Depolarisation des ventrikulären Myokards beginnt dort, wo der akzessorische Leitungsbahn in den Ventrikel eindringt, und der Impuls wird sich langsam ausbreiten, weil er sich außerhalb des Reizleitungssystems ausbreitet. Dies spiegelt sich im EKG als langsamer Start des QRS-Komplexes wider. Dieser Teil des QRS-Komplexes wird dann als Deltawelle bezeichnet.
- Verlängerte QRS-Dauer: Da die Deltawelle in die QRS-Intervall einbezogen ist, ist die gesamte QRS-Dauer verlängert.
Wie bei Erwachsenen weisen pädiatrische Patienten mit akzessorischen Leitungsbahnen im EKG nur eine Präexzitation auf, wenn die Impulse tatsächlich über die akzessorische Leitungsbahn geleitet werden. Bei der Mehrzahl der Patienten erfolgt die Überleitung über den akzessorische Leitungsbahn intermittierend, was bedeutet, dass eine Präexzitation möglicherweise nicht zu jeder Zeit zu beobachten ist.
Wolff-Parkinson-White-Syndrom
Patienten mit Anzeichen einer Präexzitation und rezidivierenden Tachyarrhythmien haben das sog. Wolff-Parkinson-White-Syndrom.
Die für das WPW-Syndrom spezifische Tachyarrhythmie ist die AV-Reentrytachykardie (AVRT). Diese Arrhythmie wird durch einen makroskopischen Reentry-Kreislauf verursacht, der die Vorhöfe, den AV-Knoten, die akzessorische Leitungsbahn und die Ventrikel umfasst. In den meisten Fällen wird der Reentry-Kreislauf durch eine supraventrikuläre Extrasystole induziert.
Es gibt zwei Arten von AV-Reentrytachykardie bei Kindern: orthodrom und antidrom. Bei der orthodromen AV-Reentrytachykardie zirkuliert der Reentry-Impuls in antegrader Richtung durch den AV-Knoten. Bei der antidromen AV-Reentrytachykardie bewegt sich der Impuls in retrograder Richtung durch den AV-Knoten.

Die Reizweiterleitung über die akzessorische Leitungsbahn kann bereits bei Geburt vorhanden sein. Die Überleitung erfolgt in der Regel intermittierend, was bedeutet, dass die Deltawellen nicht immer sichtbar sind. Darüber hinaus sind einige akzessorische Leitungsbahnen nur in der Lage, von den Ventrikeln zu den Vorhöfen überzuleiten. Diese Patienten zeigen keine Hinweise auf eine Präexzitation im Ruhe-EKG, können jedoch Tachyarrhythmien haben. Diese Art von WPW-Syndrom wird als verborgenes WPW-Syndrom (engl. concealed WPW syndrome) bezeichnet.
Neben den klassischen EKG-Merkmalen der Präexzitation können auch folgende Befunde zu sehen sein:
- Fehlen von septalen q-Wellen in den Ableitungen V5 und V6.
- Abweichung Herzachse nach links
Diese beiden Befunde können bei Grenzfällen sichtbar sein (z.B. wenn das PQ-Intervall grenzwertig signifikant ist). Für Einzelheiten siehe Perry et al.
Perry et al: Clues to the electrocardiographic diagnosis of subtle Wolff-Parkinson-White syndrome in children. J Pediatr 117:871, 1990.
Die Prävalenz des WPW-Syndroms bei pädiatrischen Patienten liegt bei etwa 0,1% bis 0,2%. Die Prävalenz ist bei Kindern mit angeborener Herzerkrankung höher. Es wird empfohlen, eine Echokardiographie bei Kindern mit Anzeichen einer Präexzitation durchzuführen.
Es ist zu beachten, dass Digoxin und Verapamil, welche die Refraktärzeit der akzessorischen Leitungsbahn verkürzen, nicht an Patienten mit Anzeichen einer Präexzitation gegeben werden dürfen, da diese Medikamente die Reizweiterleitung über die akzessorische Leitungsbahn erhöhen können. Darüber hinaus ist Adenosin bei Patienten mit unregelmäßigen Breitkomplex-Tachyarrhythmien kontraindiziert. Diese Arrhythmien können durch präexzitiertes Vorhofflimmern verursacht werden und Adenosin kann zu einem vollständigen AV-Block führen, der anschließend zu Kammerflimmern führt (Einzelheiten siehe Präexzitation, Wolff- Parkinson-White-Syndrom).
Ursachen für einen variierendes PQ-Intervall
- Wandernder atrialer Herzschrittmacher (engl. wandering atrial pacemaker, WAP): verursacht durch das Abfeuern mehrerer ektopischer Vorhofherde, was zu P-Wellen mit unterschiedlicher Morphologie führt.
- Multifokale Vorhoftachykardie (engl. multifocal atrial tachycardia, MAT): Ähnlich wie WAP, verursacht jedoch Tachykardie.
- AV-Block II Typ 1 (Wenckebach-Block)
Der QRS-Komplex
Elektrische Achse (Herzachse)
Die meisten Neugeborenen haben eine elektrische Achse von mehr als 135° (98%-Konfidenzintervall 58° bis 168°). Nach der Geburt normalisiert sich die elektrische Achse allmählich (wenn der linke Ventrikel größer wird), was bedeutet, dass sie zwischen -30 und +90° fällt. Ursachen für die Achsabweichungen werden im Folgenden erörtert.
QRS-Dauer
Die QRS-Dauer sollte in der Ableitung mit dem längsten QRS-Intervall gemessen werden (was normalerweise eine Ableitung mit sichtbarer Q-Welle ist). Bei der Geburt beträgt die QRS-Zeit <80 ms und nimmt dann nach und nach zu. Die kurze QRS-Zeit bei pädiatrischen Patienten ist auf die relativ geringe Myokardmasse zurückzuführen. Während der kindlichen Entwicklung nimmt die ventrikuläre Masse zu und die QRS-Dauer wird länger. Bei Erwachsenen bedeutet eine längere QRS-Dauer, dass die Depolarisation der Ventrikel pathologisch langsam ist. Dies kann bei folgenden Krankheitszuständen der Fall sein:
- Schenkelblöcke (RSB, LSB)
- Unspezifische intraventrikuläre Überleitungsverzögerung
- Präexzitation
- Hyperkaliämie
- Ventrikuläre Rhythmen
- Nebenwirkungen von Medikamenten
Eine Diagnose eines Schenkelblocks (RSB oder LSB) wird gestellt, wenn die QRS-Dauer 20% über der altersspezifischen oberen Normalgrenze (98. Perzentil) liegt. Wenn der QRS-Intervall größer als das 98. Perzentil ist, jedoch nicht um 20% über diesem liegt, wird die Diagnose eines inkompletten Schenkelblocks gestellt. Wenn der QRS-Intervall verlängert ist, die QRS-Morphologie jedoch weder mit einem rechten noch mit einem Linksschenkelblock kompatibel ist, kann die Diagnose einer unspezifischen intraventrikulären Überleitungsverzögerung gestellt werden, sofern andere Ursachen für eine verlängerte QRS-Dauer ausgeschlossen wurden.
Da Schenkel- und Faszikelblöcke bei gesunden Kindern äußerst selten sind, sollte das Vorhandensein dieser Defekte zu einer gründlichen kardiologischen Abklärung führen. Mehrere angeborene Herzerkrankungen können zu Schenkel- und Faszikelblöcken führen. Bei der Ebstein-Anomalie wird der Rechtsschenkelblock typischerweise von einem verlängerten PQ-Intervall begleitet.
R-Welle und S-Welle
Bei Geburt ist die R-Wellen-Amplitude in V1-V3 hoch, was durch den großen rechten Ventrikel erklärt wird. Die Amplitude der R-Wellen in V1-V3 nimmt mit zunehmendem Alter allmählich ab, während die Amplituden der R-Wellen in V4-V6 zunehmen, weil der linke Ventrikel größer wird. Im Alter von 6 Monaten sind die R-Wellen in V3-V4 normalerweise am höchsten. S-Wellen zeigen die entgegengesetzte Entwicklung (d.h. die Tiefe nimmt in V4-V6 allmählich ab und steigt in V1-V3). Es ist zu beachten, dass die S-Wellen bei Geburt tendenziell tief in Ableitungen V1-V2 liegen, trotz hoher R-Wellen (dies ist bei Erwachsenen nicht zu sehen). In ähnlicher Weise sind die S-Wellen in V4-V6 ausgeprägt und können 10 mm tief sein.
Die Amplitude der R-Wellen und S-Wellen sollte beurteilt werden. Zusätzlich kann das R/S-Verhältnis, das die Amplitude der R-Welle durch die Amplitude der S-Welle dividiert, berechnet werden. Bei Geburt ist das R/S-Verhältnis in Ableitung V1 größer als 1 (was einfach bedeutet, dass die R-Welle größer als die S-Welle ist). Das R/S-Verhältnis in V1 sollte bis zum Alter von 3 Jahren >1 betragen. Es ist selten, dass Patienten mit strukturell normalen Herzen nach 5 Jahren ein R/S-Verhältnis >1 in V1 haben.
R-Wellen mit Kerbung sind in Ableitung V1 häufig. Solche Kerbungen werden normalerweise nach einem Alter von 1 Monat gesehen (Chia et al).
Chia et al: Cardiac time intervals of normal fetuses using noninvasive fetal electrocardiography. Prenat Diagn 25:546, 2005).
Ursachen für eine hohe R-Wellen-Amplitude (Hochvoltage)
- Linksventrikuläre Hypertrophie (V4-V6)
- Rechtsventrikuläre Hypertrophie (V1-V3)
- Präexzitation
- Rechtsschenkelblock (V1-V3)
- Linksschenkelblock (V5—V6)
Ursachen für eine niedrige R-Wellen-Amplitude (Niedervoltage)
- Hypothyreose
- Perikardflüssigkeit, Tamponade
- Myokarditis
- Normalvariante
Q-Welle
Neugeborene haben normalerweise Q-Wellen in V5-V6 (septale q-Wellen) an. Die Amplitude dieser Q-Wellen variiert mit dem Alter. Ältere Kinder zeigen auch Q-Wellen in den inferioren Ableitungen an (II, III, aVF). Über die Altersspanne hinweg sind normale Q-Wellen <30 ms lang und die Amplituden überschreiten selten 5 mm (obwohl normale Q-Wellen insbesondere in Ableitung III bis zu 10 mm betragen können).
Q-Wellen in V1-V3 (QR-Komplexe) sind immer pathologisch. QR-Komplexe in V1-V3 deuten auf eine rechtsventrikuläre Hypertrophie hin. Das Fehlen von septalen q-Wellen in V5-V6 deutet auf einen Linksschenkelblock (vorausgesetzt, die die QRS-Dauer ist verlängert). Ungewöhnlich tiefe Q-Wellen deuten auf eine Hypertrophie hin. Wie bei Erwachsenen können abnormale Q-Wellen durch einen Myokardinfarkt verursacht werden, obwohl dies bei Kindern sehr selten ist, es sei denn, sie haben eine familiäre Hypercholesterinämie oder die Kawasaki-Krankheit.
Das Vorhandensein von Q-Wellen in den Ableitungen aVL und I gilt als pathologisch. Wenn es keine Q-Wellen in den inferioren Ableitungen und stattdessen große (≥3 mm tiefe und ≥30 ms breite) Q-Wellen in aVL und I gibt, sollte eine Koronararterienanomalie vermutet werden.
Rechtsventrikuläre Hypertrophie
Das EKG hat eine geringe Sensitivität (ungefähr 20%), aber eine hohe Spezifität (ungefähr 85%) für eine Hypertrophie bei pädiatrischen Patienten (Rivenes et al, Am Heart J, 2003). Dies bedeutet, dass das EKG 20% der Fälle mit Hypertrophie erkennt und 85% derjenigen, die EKG-Kriterien einer Hypertrophie erfüllen, tatsächlich eine Hypertrophie haben. Die folgende Liste zählt die EKG-Veränderungen bei rechtsventrikulärer Hypertrophie auf:
- Abweichung der Herzachse nach rechts (altersbedingte Grenzwerte).
- Das Vorhandensein von Q-Wellen in V1 (QR-Komplex) deutet stark auf eine rechtsventrikuläre Hypertrophie hin.
- Bei schwerer rechtsventrikulärer Hypertrophie sind die R-Wellen in V1 und V4R höher als normal. Die S-Wellen in V5-V6 sind tiefer als normal.
- Das Vorhandensein von rSR‘-Komplexen in V1 deutet auf eine rechtsventrikuläre Hypertrophie hin (die QRS-Dauer sollte normal sein, ansonsten sollte ein Rechtsschenkelblock vermutet werden).
- Die S-Welle in V6 ist tiefer als 98. Perzentil.
- Das R/S-Verhältnis in V1 liegt über dem 98. Perzentil.
- Das R/S-Verhältnis in V6 liegt unter dem 2. Perzentil.
- Im Alter von 7 Tagen bis 7 Jahren ist die T-Welle in V1 und V4R normalerweise negativ. Wenn die T-Welle während dieser Zeit in V1 und V4R positiv ist, sollte eine rechtsventrikuläre Hypertrophie vermutet werden.
- Ein P pulmonale deutet auf eine rechtsventrikuläre Hypertrophie hin.
Linksventrikuläre Hypertrophie
- Abweichung der Herzachse nach links (altersbedingte Grenzwerte).
- Hohe R-Wellen in V5 und V6.
- Tiefe S-Wellen in V1 und V4R.
- Das R/S-Verhältnis in V1 und V2 ist kleiner als normal.
- Das R/S-Verhältnis in V5 und V6 ist größer als normal.
- Ungewöhnlich große Q-Wellen in V5-V6.
- ST-Senkungen und T-Wellen-Inversionen in V5-V6.
Biventrikuläre Hypertrophie
Wenn Kriterien für die linksventrikuläre und rechtsventrikuläre Hypertrophie gleichzeitig vorliegen, sollte eine biventrikuläre Hypertrophie vermutet werden.
Hypertrophe obstruktive Kardiomyopathie (HOCM)
Die hypertrophe Kardiomyopathie (HCM) ist eine genetisch bedingte Kardiomyopathie, die durch eine Hypertrophie in Abwesenheit von Bluthochdruck, Aortenklappenstenose oder anderen Ursachen für erhöhten linksventrikulären Füllungsdruck gekennzeichnet ist. In etwa 70% der Fälle verursacht die Hypertrophie eine Obstruktion des linksventrikulären Ausflusstraktes (LVOT). Die Kombination von Hypertrophie und LVOT-Obstruktion wird als hypertrophe obstruktive Kardiomyopathie (HOCM) bezeichnet.
Die HCM/HOCM kann sich bereits in der Kindheit manifestieren. Dyspnoe, Brustschmerzen, Herzklopfen, Präsynkopen/Synkopen sind häufige Symptome. Diese Patienten haben ein erhöhtes Risiko für einen plötzlichen Herztod, Herzinsuffizienz und Vorhofflimmern. Das EKG ist ein relativ sensitives Instrument zum Nachweis einer HCM/HOCM, da nur 5-10% der Patienten zu Beginn ein normales EKG haben (Veselka et al.).
Veselka et al: Hypertrophic obstructive cardiomyopathy, The Lancet (2017)
EKG-Kennzeichen einer HCM/HOCM
- Anzeichen einer linksventrikulären Hypertrophie sowie sekundären ST-T-Veränderungen.
- P mitrale
- Prominente Q-Wellen in V4, V5, V6, I, aVL, aVF, II und III. Diese Q-Wellen sind meist tiefer als 3 mm und breiter als 40 ms.
- Repolarisationsstörungen (ST-T).
- Abweichung der Herzachse nach links
- Riesige T-Wellen-Inversionen in den Brustwandableitungen. Dies deutet auf eine apikale Hypertrophie hin.
- Ein Holter-EKG kann supraventrikuläre Arrhythmien (insbesondere Vorhofflimmern), ventrikuläre Rhythmen und ventrikuläre Tachykardien aufdecken. Supraventrikuläre und ventrikuläre Extrasystolen sind ebenfalls häufig.
- Eine Präexzitation ist häufiger bei Patienten mit HCM/HOCM, aber das PQ-Intervall kann auch verlängert sein.
- Leitungsstörungen sind bei der HCM/HOCM relativ häufig.

Die ST-Strecke
Die ST-Strecke ist normalerweise isoelektrisch und geht graduell in die T-Welle über. Bei gesunden Kindern sind manchmal ST-Senkungen <0,5 mm in den Extremitätenableitungen zu sehen. Gesunde Kinder zeigen selten ST-Senkungen in den Brustwandableitungen. Wie bei Erwachsenen sind ST-Senkungen mit horizontaler oder absteigender ST-Strecke alarmierender als aufsteigende ST-Senkungen. Aufsteigende ST-Senkungen sind bei hohen Herzfrequenzen normal.
ST-Hebungen können bei Kindern, insbesondere Jugendlichen, auftreten. ST-Hebungen sind am häufigsten in den Brustwandableitungen (V2-V6) und können 2 mm erreichen (gemessen im J-Punkt). Die häufigsten Ursachen für ST-Streckenhebungen sind wie folgt:
- Normale ST-Streckenhebung
- Frühes Repolarisationssyndrom
- Perimyokarditis (Myokarditis)
Die normale ST-Streckenhebung und die frühe Repolarisation (early repolarisation) manifestieren sich in gleicher Weise bei Kindern und Erwachsenen.
Ein akuter Myokardinfarkt ist bei Kindern selten. Ischämische ST-Hebungen bei Kindern ähneln denen bei Erwachsenen. Die Perimyokarditis (Myokarditis) ist jedoch die häufigste Ursache für Brustschmerzen mit ST-Hebungen bei Kindern. Hyperkaliämie, ein Pneumothorax sowie Koronararterienanomalien können ebenfalls ST-Hebungen verursachen.
T-Welle
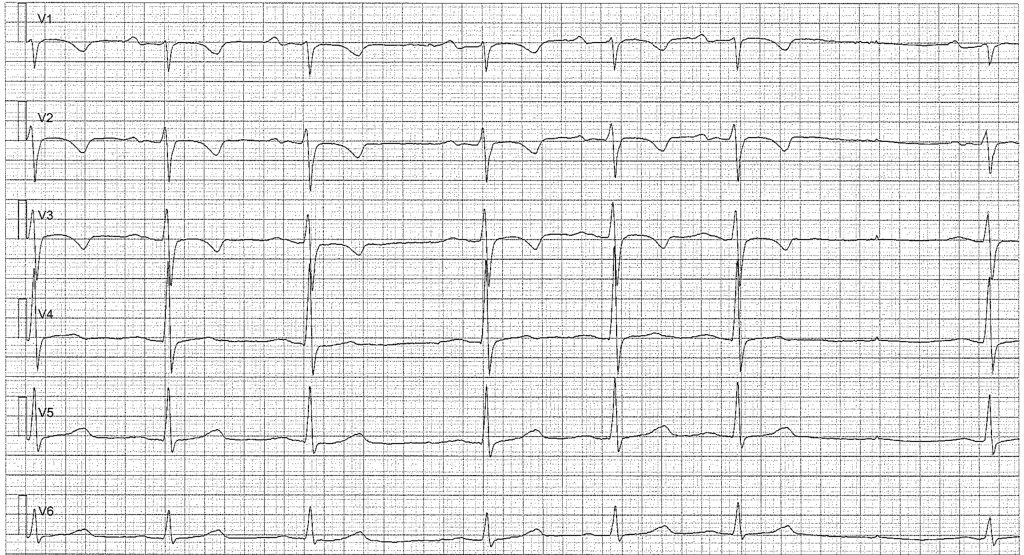
Bei Geburt sind die T-Wellen in den Ableitungen V3R und V1 positiv, aber innerhalb von 7 Tagen werden sie invertiert (negativ). In den meisten Fällen werden die T-Wellen auch in V2 und V3 negativ. Diese T-Wellen-Inversionen bestehen bis zum Alter von 10 Jahren (manchmal bis zu 15 Jahren). Daher sind T-Wellen-Inversionen in den Ableitungen V3R, V1, V2, V3 zwischen 7 Tagen und 10 bis 15 Jahren normal. Das Fehlen von T-Wellen-Inversionen in diesen Ableitungen sollte zum Verdacht auf eine rechtsventrikuläre Hypertrophie führen. Nach dem Alter von 10 bis 15 Jahren werden die T-Wellen allmählich positiv (dies beginnt in Ableitung V3 und bewegt sich allmählich in Richtung Ableitung V3R). Einige Kinder zeigen weiterhin eine negative T-Welle in V1, und dies ist ein Normalbefund (die T-Wellen-Inversion steht konkordant mit dem QRS-Komplex, der in Ableitung V1 ebenfalls negativ ist). Siehe Abbildung 7.

Ein juveniles T-Wellenmuster wird diagnostiziert, wenn sich die T-Wellen nach der Pubertät nicht normalisieren (d.h. fortgesetzte T-Wellen-Inversionen in den Ableitungen V1-V3).
Eine globale T-Wellen-Inversion besteht, wenn die T-Wellen in allen Brustwandableitungen ohne Anzeichen einer Herzerkrankung im Erwachsenenalter und darüber hinaus invertiert sind.
Ursachen für hohe, flache und negative T-Wellen bei Kindern sind die gleichen wie bei Erwachsenen.
U-Welle
Die Beurteilung der U-Welle bei Kindern unterscheidet sich nicht von der bei Erwachsenen. Sie kommt gelegentlich, meist während einer langsamen Herzfrequenz, in den Ableitungen V2-V4 vor.
QT-Dauer (QTc)
Das QT-Intervall spiegelt die Gesamtdauer der ventrikulären De- und Repolarisation wider. Dies entspricht dem Intervall vom Anfang des QRS-Komplexes bis zum Ende der T-Welle. Da die QT-Dauer invers mit der Herzfrequenz zusammenhängt (die QT-Dauer wird bei höheren Herzfrequenzen kürzer), muss der QT-Interval an die Herzfrequenz angepasst (korrigiert) werden. Dies wird als korrigierte QT-Dauer (auch QTc-Dauer für engl. corrected QT interval) bezeichnet.
Die Beurteilung der QTc-Dauer ist sehr wichtig, da eine verlängerte QTc-Dauer das Risiko für maligne ventrikuläre Arrhythmien und einen plötzlichen Herztod (Long-QT-Syndrom, LQTS) erhöht. Das automatisch berechnete QTc-Dauer sollte immer durch manuelle Berechnung überprüft werden (Miller et al: Diagnostic accuracy of screening electrocardiograms in long QT syndrome I. Pediatrics 108:8, 2001). Die manuelle Messung des QT-Intervalls sollte in den Brustwandableitungen erfolgen. Das Intervall wird vom frühesten QRS-Ausschlag (in jeglicher Ableitung) bis zum Ende der T-Welle (in jeglicher Ableitung) gemessen. Dies bedeutet, dass der Beginn des Intervalls z.B. in Ableitung V2 und das Ende in Ableitung V5 definierte werden kann. U-Wellen sollten nicht mit in die Messung einbezogen werden. Sobald das QT-Intervall gemessen wurde, wird es mit der Formel von Bazzet auf die Herzfrequenz korrigiert:

Ursachen für eine verlängerte QTc-Dauer
- Hypokaliämie
- Hypokalzämie
- Hypothermie
- Nebenwirkungen von Medikamenten
- Schlaganfälle
- Ketogene Diät
- Akuter Gewichtsverlust
- LQTS
- Perikarditis, Myokarditis, Perimyokarditis
Die Prävalenz des LQTS beträgt 0,05% bei Kindern. Für Einzelheiten siehe bitte Long-QT-Syndrom (LQTS). LQTS kann eine oder mehrere der folgenden EKG-Veränderungen verursachen:
- Lange QTc-Dauer
- Alternierende T-Welle: Die Amplitude der T-Welle variiert von Schlag zu Schlag.
- Abnormale T-Wellen-Morphologie.
- Bradykardie.
- Torsade de pointes.


Es ist zu beachten, dass Kinder mit LQTS gelegentlich eine normale QTc-Dauer haben. In der Regel gilt: Je länger die QTc-Dauer ist, desto gefährlicher ist der Zustand. Bei einer QTc-Dauer von 500 ms besteht ein signifikantes Risiko für ventrikuläre Arrhythmien und bei 600 ms besteht ein sehr hohes Risiko.
Die Mortalität bei LQTS ist sehr hoch, wenn der Zustand unbehandelt bleibt. Die 5-Jahres-Mortalität beträgt 10% (Schwartz PJ et al). Die genetischen Ursachen und die Behandlung des LQTS wurden zuvor diskutiert. Das LQTS ist normalerweise erblich, kann aber als De-Novo-Mutation auftreten. Einige Mutationen zeigen eine geringe Penetration, weshalb Eltern die Mutation trotz einer normalen QTc-Dauer haben können.
Es sollte auch beachtet werden, dass nicht alle Kinder mit einem verlängerten QTc-Intervall in einer (einzigen) EKG-Aufzeichnung unbedingt ein LQTS haben. Das Management von pädiatrischen Patienten mit verlängerter QTC-Dauer wird in den hier verfügbaren europäischen Leitlinien ausführlich diskutiert.
Schwartz PJ et al, in Zipes DP et al: Cardiac electrophysiology: from cell to bedside, 3rd edn. Philadelphia: WB Saunders, 2000:597-615
Differentialdiagnosen bei einer verkürzten QTc-Dauer
Eine verkürzte QT/QTc-Dauer ist mit einem erhöhten Risiko für eine ventrikuläre Tachykardie assoziiert. Es gibt drei Ursachen für eine verkürzte QTc-Dauer:
- Hyperkalzämie
- Digoxin
- Angeborene verkürzte QTc-Dauer (Short-QT-Syndrom), was sehr selten ist.

